乳腺癌:早期检测 据估计,217640的乳癌新病例被诊断患有今年美国,超过99%,其中乳腺癌的妇女发生。乳腺癌是美国妇女最常见的恶性肿瘤,它是第二大死因从(肺癌是美国第一位女性癌症)。一个女人一生中的风险(80年寿命,患乳腺癌的)为12.5%,即8 1。早期乳腺癌检测已经证明,以减少死亡率。技术的不断发展,以提高检测的准确性。 本文件的目的是讨论当前乳腺癌筛查指导理念和评价方面的证据筛查技术。报告还重点作为筛选工具,以确定非显而易见的乳腺病变检测技术等。此信息是为了帮助在作出有关决定适当的护理工作者。在实践中的变化,可能需要根据个别病人的,资源的需要,并限制特有的机构或做法的类型。 风险因素: 流行病学的分析-为什么妇女获得乳腺癌了解较少。几个因素已查明的风险增加,如:乳腺良性疾病,遗传因素,饮食,外源激素,酒精和烟草的消费,乳房创伤和病毒。乳腺癌的风险增加了作为一个女人和日益老龄化,70%以上的癌症发生年龄50岁。家族历史,主亲属(母亲,姐妹或女儿患乳腺癌)的风险增加。其他因素有:早发月经(岁前获得期限12年),从未生育或第一次怀孕岁以上的30年中,超过40以上的理想体重和接触滴滴涕(农药),印刷电路板,或过度%称重辐射胸壁。 有几项研究表明,最重要的,在后来的发展病理癌危险因素的程度和性质(典型或非典型)的上皮细胞增殖。 乳腺病理诊断分组癌的风险(1):
乳腺癌普查筛选工具仅作为有效的能力,以帮助预防疾病。理想的检查方法,应找出与癌症生物学与发展有关的统计意义的变化。这也应适用于一个合理比例的高危人群,并应微创。此外,有效的干预和预防措施应该可用。为更好的方法预防乳癌和侦查搜索在继续,已与子宫颈癌的发生与死亡率显着降低的目标。 产科医生和妇科医生在一个有利的地位来诊断乳腺疾病的病人。为实现这一初始步骤是通过视觉检查和乳房触诊检查,并应组成部分,初步完成所有的产科和妇科检查。应指示患者在生命的技术,长周期的自我乳房检查和自我的重要性,告知检查。 乳房自我检查(疯牛病):尽管在支持或反对自我检查乳房(疯牛病),自我检查乳房的缺乏肯定的数据有可能发现明显乳腺癌和应建议。乳腺癌是最自我发现的癌症。事实上,在美国大多数乳腺癌患者被发现的触诊。乳房自我考试(疯牛病)应在一个舒适的房间,其中包含一个(包括一个枕头床),一面镜子,良好的照明。您可能会执行疯牛病当您在淋浴是,有些女性发现湿手在检测乳房的变化有所帮助。请记住执行疯牛病而躺在除了站起来了。乳房是动态的机关和可能发生的变化,每月和整个生命阶段(青春期,生育,更年期)。美国食品和药物管理局已批准,旨在改善触觉疯牛病艾滋病。这是一个好主意,画一幅你觉得在你的疯牛病素描和纪念您的日历。 请记住,大多数乳房肿块不是癌。事实上,据估计,只有11块一个是肿瘤。疯牛病是免费的,无毒的,有些医生认为,疯牛病的帮助赋予妇女权力,利用自身的健康管理。适当每月乳房自我检查,之后月经周期与临床乳房检查由训练有素的医护人员结束几天每年一次,提出了建议。 对乳房自我步骤考试乳房X光摄影:对诊断患有乳腺癌的妇女中大多数人没有明显的危险因素。 1966年,麦克唐纳估计侵袭性乳腺癌倍增时间的范围从23到209天,为128个本地化癌症和肿瘤的转移时间平均85天。基于数学计算的100天的倍增时间为基础的图形显示,一个8岁的临床前阶段,为期4年的乳腺癌的增长,这在以前是诊断乳腺癌的发生一般大小的临床阶段。乳腺X线检查可能确定非大约1毫米的肿块,以1厘米,在其临床前阶段的三年,才具有明显的(2)。大多数研究的乳腺作为最终用途死亡率点,所以检查的价值往往是单纯的死亡率为基础。一些研究考虑到生活质量的事实,在早期阶段进行治疗少发病的早期检测效果。 1982年,乳腺癌检测示范项目建立了与乳腺癌的乳房X线检查,以确定适用于非明显病变。 5年的结果表明,8.7%的乳腺癌患者是由只,41.6%是由只,和47.3%,但都被乳房X光检查和身体检查发现乳房X光检查发现体检发现。乳腺癌的浸润小于1厘米,52.6%,只有通过检测乳腺。他们之间的乳腺癌检测和治疗,10年生存率为79%(3)妇女的4,240。 在健康保险计划和大纽约,估计导致乳腺癌检测示范项目数据时的基础上(对乳腺检测之间的时间,当病变临床检测的浸润性乳腺癌)为1.7年(范围:0.4 -3年),这表明最佳筛查间隔将不超过1.7年。甄别乳腺临床试验有年龄上限标准,从64-74年不等的多数。医疗合作的发病率和预期寿命应在乳腺癌审议筛选年龄在75岁或年纪较大的妇女计划的好处,因为对风险的甄别乳腺转移的比例继续随着年龄的不利影响。阿的建议达成共识不存在。然而,荟萃分析的结论是,检查年龄在70-79岁的妇女乳房X光检查是中等成本效益和产量预期寿命(3)略有增加。 建议乳腺癌筛查:
对筛选乳腺不利后果: 对辐射的危险最初关切(例如,乳腺癌诱导辐射)基本上已经消除在乳房X线照相技术,技术的改进和临床经验。假(即与被认为需要进一步评估这些积极的乳房X光异常,确认病灶不是癌症)是一个持续的关注。假阳性检查乳房X光摄影需要与补充意见,超声诊断乳房X光检查,甚至活检在20-30%的情况下,试图达成一项准确的诊断。乳腺X线的检查已经确定,审查和这些心理,行为及的生活质量问题似乎内在要求乳腺癌的恐惧心理后果。 其他筛选技术: 超声是一个既定的附属物,在乳房X线成像评价。它是有用的评价定论X线表现,评估和年轻患者乳房组织致密其他妇女组织的指导核心针穿刺活检和其他活检技术,并区分了坚实的群众囊肿。细针穿刺细胞学检查,尤其是在欧洲已取代乳腺异常的评价切除活检。许多时候,最终的诊断是不可能的,主要是因为它无法分辨侵入从在原位癌。立体定向引导穿刺活检(CNB)的,它使用大口径针,似乎有几个优点,细针穿刺细胞学检查。捷克共和国国家银行是便宜得多切除活检,在更短的发病率结果,并没有留下明显的疤痕。某些良性病变有一个共存癌发病率相对较高,以及与它的体积小,神州商务组织可能不足以排除癌症。 磁共振成像可以成为一个有用的辅助诊断乳房X光检查,但成本,考试时间和造影剂注射禁止其作为常规,人口为基础的筛选技术的使用。彩色多普勒超声,电脑辅助检测,正电子发射断层,scinti,乳腺,继斜X线照相和热成像显示在具体的承诺,但选择的情况仍在临床调查,并没有提出有效的筛选技术。 导管在乳腺癌检测灌洗: 尽管目前的成像研究已经证明在确定恶性肿瘤有效,他们有能力有限,检测原位病变。乳管内视是侵入性,需要镇静和麻醉。各种手续,可获取,如乳头吸液(标准二进制),随机乳晕细针穿刺收集导管上皮细胞进行评估,并导管,灌洗。乳房乳头的平均包含8点55牛奶毛孔。每个孔延伸到中央管,这侧小叶单位,其中奶哺乳过程中产生的。在终端导管小叶单位在牛奶生产,哺乳期间,小叶结束。研究建议,是重要的细胞异型生物标志物前面最恶性病变,是高度发展的预测乳腺癌。由于理论,积极管道更容易产生细胞,患者也应选择是基于自己的能力产生了温和的愿望乳头吸液的愿望(标准二进制)。这个过程还确定了流体口高产灌洗管道。 要执行导管灌洗,局部麻醉的应用,而导管孔口以灵活微导管空心。麻醉,然后注入往往通过向麻木管道导管。注入生理盐水冲洗是通过导管小叶单位,然后将液体收集。试样准备标准巴氏染色,细胞学和评价。导管灌洗应结合使用的,而不是代替,临床乳房检查和乳房X线照相。美国癌症协会(ACS)认为,乳腺导管灌洗可在帮助高危病人小组,以进一步评估其风险,并决定如何将它莫西芬,激素治疗,外科手术预防有用。乳腺癌的外科医生协会也发表了一份正式声明,支持导管灌洗。 乳腺癌基因筛选: 细胞有两个副本- BRCA1和BRCA2,他们是肿瘤抑制基因。这些基因的蛋白产物相互交流的途径其他修复受损的DNA。 BRCA1基因- 2突变增加癌症的风险比其他因素,而这些突变增加早发性乳腺癌的风险。尽管估计50-80%的乳腺癌患者寿命为那些谁携带BRCA1或BRCA2基因突变的风险,很少有任何建议人口变化为基础的筛选,在这个高危险群乳腺准则。确认没有监测数据或相关的临床试验是BRCA1或BRCA2电信运营商提供的癌症遗传研究联盟已提出第三级临时建议1)教育工作,每月自我检查乳房,2)年度或半年度临床乳房自我检查开始时年龄25-35岁,3)在每年的乳房X线照相时代的开始25-35岁(4)。 吸取的经验教训易感基因检测:
对BRCA1基因与2肯纳兹人口突变发生率为1 / 40和非德系的人口是1 / 400到1 / 800。如果所有的妇女进行甄别德系的BRCA基因突变的创始人?赞成的理由是:它确定突变运营商早期,导致预防或早期诊断。基因歧视是不会成为问题。反对的论据是:假阴性只要创始人突变筛选和虚假的安全感对那些消极的,谁进行测试基线患癌症的风险。 保险范围是广泛使用的基因测试。 97从2000-2001年完成了保险索赔%的报销94%的平均偿还。很多保险公司都制定了准则,以确定咨询和检测的资格。现在医疗保险支付测试。好处是:它提供了风险,为个人和家庭信息,提供信息,医疗保健和有用的结果的不确定性和可缓解焦虑。限制是:1负的结果是最权威的,如果有一个家庭已知突变。有些遗传变异是未知的临床意义。 化学预防:对于如何预防乳腺癌的搜索已经进行了很多年。他莫昔芬(1 triphenylethylene),这是一种抗雌激素虽然是化学性质相关的一种雌激素,是第一次真正的选择性雌激素受体调节剂。目前已超过了作为一个与乳腺癌患者的辅助三苯氧胺四分之一世纪的经验。由于数据显示,在对侧乳腺癌的接受与不接受他莫昔芬的,一个大型乳腺癌预防试验(P - 1型),他莫昔芬的妇女发展的大量保护开始于1992年(国家外科辅助乳房项目[NSABP] /化学实验室) 。在盖尔模式,是估计算法患乳腺癌的风险,确定高风险。盖尔模型的目的是为妇女的乳房X线每年筛选程序。 盖尔模型来确定患乳腺癌的风险(5):
该模型预测,在5年或预期寿命为乳腺癌的风险。最近,其他选择性雌激素受体调节剂,已成为评价提供;雷洛昔芬是一个最广泛研究。这种药物主要是用来确定在雷洛昔芬的评价结果参与者多绝经后骨质疏松的预防(更多)谁是3年治疗。侵入性乳腺癌的风险为76%,比安慰剂组的雷洛昔芬组低。这是由于在发展的雌激素减少90%,受体阳性肿瘤。这些结果导致他莫昔芬和雷洛昔芬(名人)的研究在谁在为这种疾病的高风险绝经后妇女乳腺癌的预防癌症的这些药物的评价试验。 其他可能的风险估值和诊断工具: 非典型增生:它发生在早期构成转型过程中的恶性表型的组织学连续变化过程。阿病理或细胞学不典型性的发现是一对患乳腺癌的危险因素强劲。风险增加一倍以上的妇女患乳腺癌家族史(相对危险度:异型性,仅〜5;异型+家族史,11-18),大约40%将这些妇女在其一生中发展乳腺癌。不典型增生可作为一个罹患乳腺癌的风险估计,因为大多数乳腺癌患者随后在5诊断(6)年内出现。 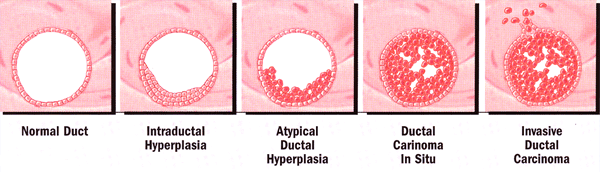 乳腺增生的发展侵入性疾病 乳腺X线密度:对妇女的乳房密度可以评价例行X光,并已被证明与患乳腺癌的风险相关。乳腺实质的模式(乳房密度)是指结缔组织和腺体组织数额相对乳房脂肪组织。由于乳腺癌也是组织致密,乳房密度高的乳房X线照相组成可以掩盖肿瘤,防止其早期发现。乳房密度高,亦是乳癌的危险因子,但可能是雌激素或雌激素接触独立受体地位(7)。因此,乳房密度与乳腺癌有关的风险增加也可能来自于非胰岛素,如雌激素水平的因素,如生长因子,饮食,和/或遗传和环境因素。乳房密度有很大的妇女,可以有高(〜63%)的遗传。计算机X线图像的纹理分析表明,在高风险的妇女谁携带BRCA1或BRCA2基因突变的实质模式的高密度,粗糙,并降低少于这些妇女发展为乳腺癌(8低风险的地方差异对比) 。 组织学和细胞学乳腺癌的风险分析:在正常的细胞检测乳腺癌已被证明是乳腺癌的危险因素。有很多各种不同的方法获得由乳房样本。收集的组织学和细胞学分析-细针抽吸(FNA),乳头抽吸,穿刺活检和手术活检细胞的传统方法-所有有局限性(9)。随机取样的细针穿刺,例如,侵入性程序,并经常组织产量不足进行分析,特别是老年妇女。同样,乳头抽吸细胞通常包含有不足。穿刺活检和手术活检产量充足,但侵入细胞的程序,不会只进行风险评估。较新的,低侵入性方法病理或细胞学分析导管灌洗,这是一种微创手术导管的提取液使用局部麻醉,可以在门诊中进行的使用。对乳腺导管灌洗可能的候选人是谁,由盖尔模型预计将在妇女对乳腺癌的风险增加。 乳腺成像:它一直在预测诊断乳腺癌的可能性的工具。乳腺影像报告和数据系统(双向回返数据库),由美国放射学院,规范化的图像评估开发帮助确定适当的跟进。可疑异常-病变,要求干预(例如,活检),但不一定恶性肿瘤-被分配到第4类。在研究进行评估作为对智能辅助,美国放射学会的评分中,妇女有4类病变及高架5年盖尔的盖尔风险模型的使用("1.7%)已在比那些恶性得多活检结果第四类病变和低盖尔风险(42%比21%,误差".0001;相对危险度1.94)。研究人员猜测,方法可能是最有益的应用双向美国放射学会的3类病变,但妇女在这一类数字太分析(10)小。乳腺癌的影像作为对加强风险评估模型盖尔辅助使用需要进一步的分析。 改善与建议的情况: 根据行为理论,一个高风险的认识将提高筛检,而低风险的看法会产生相反的效果。虽然这是在很多情况下真正的问题是复杂的。研究发现,减少女性的知觉风险并没有影响她打算取得乳房,并可能增加,检查建议的情况。乳腺癌有关的心理困扰(例如,严重忧虑)已建议与检查相关的依从性差,甚至在确定了妇女在高风险,而温和的担心,是具有较高的相关检查的可能性。据发现,担心与乳腺癌发病率和乳房X光摄影的关系得到与一个倒U形图案有关。与中等水平的担心妇女更有可能定期乳房X线照片比那些担心水平也很少,甚至非常高。研究人员的理论认为,引发严重的忧虑,而温和的关注,警惕和动机否认和回避行为,使用筛选方法(11)。遗传咨询,可以提供家庭历史的关键评估,以帮助确定一个遗传性癌症易感综合征的可能性和在基因测试是否适当。承运人对突变后的临床建议需要考虑到病人的年龄,为今后的生育愿望,历史的和其他的医疗检查时,处方干预或预防性手术(12)。对癌症易感基因检测的实际应用有能力减少挽救生命遗传性癌症的负担,降低医疗发病率,减少心理压力。 遗传性乳腺癌和卵巢癌:遗传性乳腺癌和卵巢癌是一种遗传性癌症的易感性综合症。此综合征的特点是与乳腺癌或卵巢癌或两者多个家庭成员,在一个人的存在两种乳腺癌和卵巢癌和乳腺癌发病年龄早(通常在50岁前)。遗传性乳腺癌和卵巢癌的绝大多数是由于更改或突变无论是在BRCA1或 BRCA2基因。这些突变可以继承或母亲或父亲。目前的战略,以减少发展中国家的妇女与已知的有害BRCA基因突变患乳腺癌的风险,包括监测,化学预防和治疗。推荐监视包括临床乳房检查每半年以及两个年度和年度乳房X线乳腺磁共振成像检查的时代的开始25年或更早上最早的家庭(14)发病年龄为基础的。磁共振成像更为敏感的乳腺癌患者比乳房X线照相检测,以及磁共振成像,乳房X光检查相结合,临床乳房检查已为乳腺癌的高危易感基因突变携带者的检测灵敏度最高的。风险降低输卵管卵巢切除术减少40-70%(13)对患乳腺癌的风险。这种保护可能仅当患者在绝经前的风险的时间,降低输卵管卵巢切除术。此外,研究表明,BRCA1基因突变携带者可能有从低风险的保护作用,减少卵巢切除术对乳腺癌比BRCA2突变运营商(14)癌症的风险输卵管。 重要的是高风险的个人留在经验丰富的医疗风险增加妇女在医生联系,由于迅速发展,测试技术的研究和改进。例如,在BRCA1和 BRCA2基因重排的大型测试已经开发出来,可能有助于确定在一个高风险的家庭以前测试谁对这些消极的一小部分的基因突变。阿的遗传风险评估是建议患者大于1的有遗传倾向的乳腺癌和卵巢癌的约20-25%的机会。该模型是一个盖尔验证该预算将妇女的发展,在未来5年内浸润性乳腺癌的风险的基础上讨论了上述因素的绝对风险白人妇女的工具。没有单一的工具,它可以准确预测的妇女将得到乳癌。美国国家癌症研究所乳腺癌的风险评估和风险计算器工具可在:http://www.cancer.gov/bcrisktool/ 摘要: 年龄40-49岁的妇女应该有乳腺X线检查每1-2年。 50岁的妇女和老年人应每年进行乳房X光检查。尽管在支持或反对乳房自我缺乏肯定的数据检查,自我检查乳房(疯牛病),有可能发现明显乳腺癌和应建议。所有的妇女应每年临床乳房检查作为体检的一部分。当一个非肿块是乳腺检查认为,患者应交由专业经历了乳腺癌的诊断,使一个完整的图像的工作,能有效地执行。乳房X光摄影是非常有用的评价妇女谁怀疑他们有乳腺肿块的临床医生不能触诊。在这种情况下,聚焦超声显像可能是一个完整的影像评价部分于任何年龄。阿非肿块可能需要针立体定位穿刺活检或活检。 妇女可能受益于遗传咨询和测试,如果他们的家庭的历史,包括诊断和所有类型的癌症的年龄(在任何亲戚,女性和男性),显示了他可能常染色体显性遗传模式或癌症如BRCA基因突变已被发现在他们的家庭。遗传咨询会的风险和利益的考验。 推荐阅读:
参考文献:
|